הגישה החדשנית הוכחה כיעילה בעכברי מודל – הן כטיפול מונע והן כתרופה למלנומה פעילה. פרופ’ רונית סצ’י-פאינרו, מובילת המחקר: “אנו סבורים שהשיטה שפיתחנו עשויה להתאים גם לסוגים אחרים של סרטן, וכי היא מהווה תשתית מוצקה לפיתוח עתידי של חיסונים נגד סרטן בבני אדם.”
חוקרים באוניברסיטת תל אביב, בהובלת פרופ’ רונית סצ’י-פאינרו, ראש המחלקה לפיזיולוגיה ולפרמקולוגיה וראש המעבדה לחקר סרטן וננו-רפואה בפקולטה לרפואה, פיתחו ננו-חלקיק שעשוי לשמש כחיסון נגד סרטן העור הקטלני מלנומה. החיסון הוכח כיעיל ביותר בעכברי מודל בשלושה מצבים עיקריים: כטיפול מונע, כתרופה לגידול הראשוני, ולמיגור גרורות.
במחקר השתתפו ד”ר אנה סקומפרין מהמעבדה של פרופ’ סצ’י-פאינרו ופרופ’ הלנה פלורינדו וד”ר ג’ואוו קוניוט מאוניברסיטת ליסבון אשר שהו במעבדה במסגרת שבתון וחילופי סטודנטים במשך שנה.
המאמר התפרסם בחודש שעבר בכתב העת Nature Nanotechnology .
החוקרים במעבדתה של פרופ’ סצ’י-פאינרו פיתחו חלקיקים זעירים העשויים מפולימר מתכלה, שגודלם כ-170 ננומטר. בתוך כל חלקיק הם ‘ארזו’ שני פפטידים – שרשראות קצרות של חומצות אמינו, שמאפיינים תאי מלנומה. לאחר מכן, הם הזריקו את הננו-חלקיקים לעכברי מודל שנשאו מלנומה בעור.
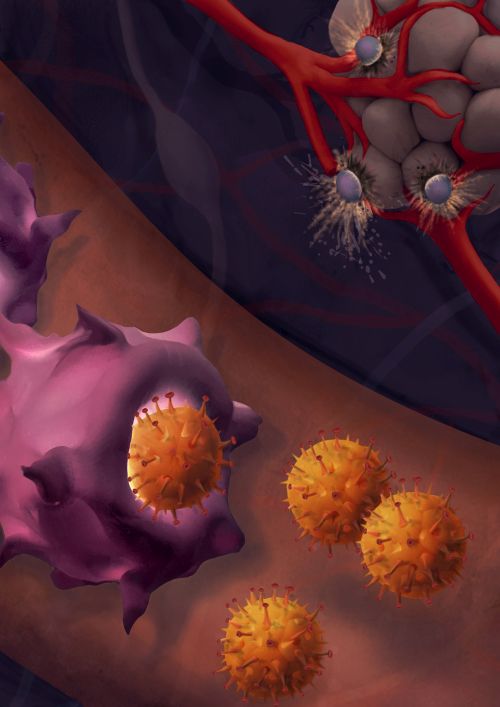
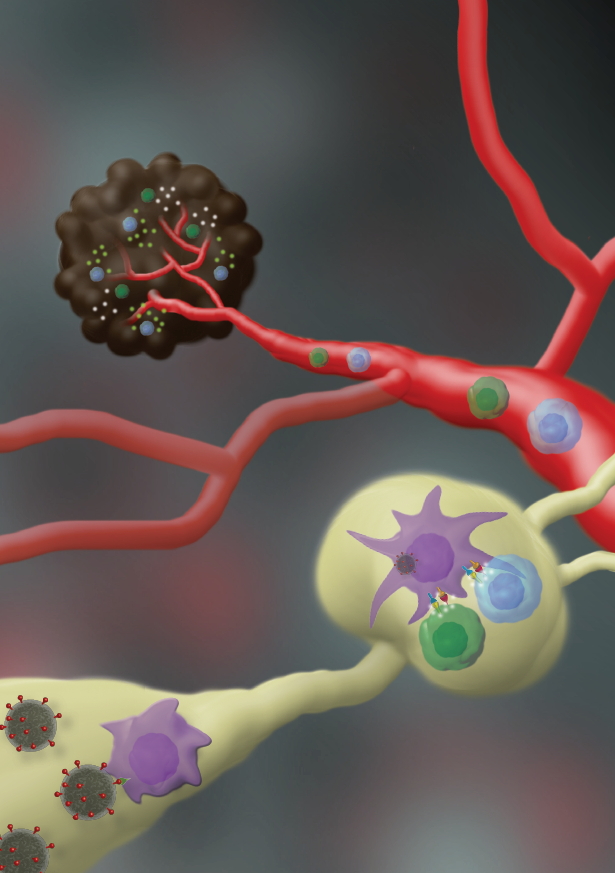
“ננו-חלקיקים אלה נושאים על גבם מולקולת סוכר המשמשת כ”ראש חץ” המכוון לתאים דנדריטים של מערכת החיסון, המפעילים תאי T שיתקפו את הגידול, מסבירה פרופ’ רונית סצ’י-פאינרו, “חלקיקים אלה פעלו בדיוק כמו החיסונים המוכרים למחלות הנגרמות על ידי נגיפים: הם עוררו את מערכת החיסון של העכברים, כאשר תאי מערכת החיסון (תאי ה-T המופעלים) למדו לזהות ולתקוף תאים המכילים את שני הפפטידים ‘הארוזים’ – כלומר את תאי המלנומה. המשמעות היא שמעכשיו, מערכת החיסון של העכבר המחוסן תתקוף את תאי המלנומה, אם וכאשר יופיעו בגופו.”
בהמשך המחקר, בחנו החוקרים את יעילותו של החיסון בשלושה מצבים שונים. ראשית, מניעה: החיסון הוזרק לעכברים בריאים, ולאחר מכן הוזרקו להם תאי מלנומה. התוצאה: העכברים לא חלו, כלומר החיסון מנע את המחלה. שנית, טיפול בגידול הראשוני: שילוב בין החיסון החדשני לטיפולים אימונותרפיים נבחן על עכברי מודל למלנומה. הטיפול הסינרגיסטי המשולב עיכב משמעותית את התקדמות המחלה, והאריך במידה רבה את חייהם של כל העכברים שטופלו. ושלישית, טיפול בגרורות: החוקרים בחנו רקמות אנושיות של גרורות מלנומה במוח שהוסרו מחולים (גרורות במוח מהוות גורם תמותה עיקרי בקרב חולים המאובחנים בשלב מאוחר), ומצאו כי הן אכן מכילות את שני הפפטידים המהווים יעד לחיסון.
בניסוי המשך נבחנת עתה יעילות החיסון בעכברי מודל למלנומה עם גרורות באזורים שונים בגוף (מוח, ריאות, כליות ועוד).
“המלחמה בסרטן בכלל, ובמלנומה בפרט, הולכת ומתפתחת לאורך השנים, באמצעות מגוון שיטות טיפוליות כמו: ניתוחים, כימותרפיה, הקרנות ואימונותרפיה; אך גישת החיסון, שהוכחה כיעילה כל כך כנגד מחלות נגיפיות לסוגיהן, טרם הוכתרה כהצלחה לטיפול בסרטן”, אומרת פרופ’ סצ’י-פאינרו. “במחקר שלנו הראינו שניתן לייצר חיסון יעיל כנגד סרטן העור מלנומה.”
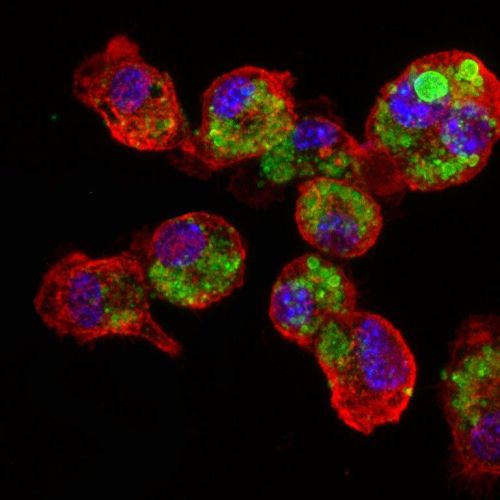

“המחקר שלנו פותח פתח לגישה חדשה לחלוטין – גישת החיסון – לטיפול יעיל במלנומה, גם בשלביה המתקדמים של המחלה,” מוסיפה פרופ’ סצ’י-פאינרו. “אנחנו מאמינים שהשיטה שפיתחנו עשויה להתאים גם לסוגים אחרים של סרטן, וסבורים שעבודתנו מהווה תשתית מוצקה לפיתוח עתידי של חיסונים נגד סרטן בבני אדם.”
המחקר מומן על ידי:
- האיחוד האירופאי במסגרת המועצה האירופית למחקר (ERC) ו-EuroNanoMed II
- פרס מטעם קרן משפחת סבן וה- Melanoma Research Alliance (MRA)
- הקרן לחקר הסרטן בישראל (ICRF)
- הקרן הלאומית למדע (ISF)

