פריצת הדרך המדעית עשויה לסייע לטיפול בילדים שסובלים מאובדן שמיעה. הטיפול החדשני מחליף גנים פגומים בגנים תקינים ועשוי למנוע חירשות בקרב ילדים שנולדים עם מוטציה גנטית הגורמת לאובדן שמיעה. החוקרים מעריכים כי בעתיד ניתן יהיה לפתח טיפולים לגנים נוספים על בסיס ממצאים אלו.
מחקר חדש מאוניברסיטת תל אביב מציג טיפול חדשני לחירשות שמבוסס על החדרת מטען גנטי לתאי האוזן הפנימית. במסגרת הטיפול, המטען הגנטי מוחדר לתוך התא הפגום בצורה כזו שהוא למעשה “מתקן” את הפגם הגנטי ומאפשר לתא להמשיך לתפקד בצורה תקינה.
במסגרת המחקר הצליחו החוקרים למנוע את הידרדרות השמיעה של עכברים עם חירשות הדרגתית. לדבריהם, הטיפול עשוי להביא לפריצת דרך בטיפול בילדים שנולדים עם מגוון מוטציות הגורמות לאובדן השמיעה.
מובילי המחקר הם פרופ’ קרן אברהם ושחר טייבר, דוקטורנט במסלול המשולב לרפואה ומחקר (MD-PhD), מהמחלקה לגנטיקה מולקולרית של האדם וביוכימיה, בבית הספר לרפואה ע”ש סאקלר, ומבית הספר סגול למדעי המוח באוניברסיטת תל אביב. כמו כן, השתתפו במחקר פרופ׳ דוד שפרינצק מבית הספר לנוירוביולוגיה, ביוכימיה וביופיזיקה בפקולטה למדעי החיים ע”ש ג’ורג’ ס’ וייז של אוניברסיטת תל אביב, ופרופ׳ ג׳פרי הולט מבית החולים לילדים בבוסטון ומבית הספר לרפואה של אוניברסיטת הרווארד. המחקר פורסם בכתב העת EMBO Molecular Medicine.

חירשות היא הליקוי החושי הנפוץ ביותר. לפי ארגון הבריאות העולמי ישנם כחצי מיליארד לקויי שמיעה כיום ומספר זה צפוי להכפיל את עצמו בעשורים הקרובים. אחד מתוך 200 ילדים נולד עם ליקוי שמיעה ואחד מתוך אלף ילדים נולד חירש. במחצית מהמקרים גורם החירשות הוא מוטציה גנטית. נכון להיום, מוכרים בספרות הרפואית כ־100 גנים שמוטציות בהם עלולות לגרום לאובדן השמיעה.
פרופ’ אברהם: “במחקר זה התמקדנו בחירשות גנטית הנובעת ממוטציה בגן SYNE4 – חירשות נדירה שהתגלתה לפני כמה שנים במעבדתנו בקרב שתי משפחות בישראל, ומאז אובחנה גם בטורקיה ובאנגליה. ילדים שיורשים את הגן הפגום משני הוריהם נולדים עם שמיעה תקינה, אך שמיעתם הולכת ומידרדרת במהלך הילדות. הסיבה לכך היא שהמוטציה גורמת לשינוי במיקום הגרעין ולמוות של תאי השערה בשבלול שבאוזן הפנימית, האחראים לקליטת גלי הקול”.
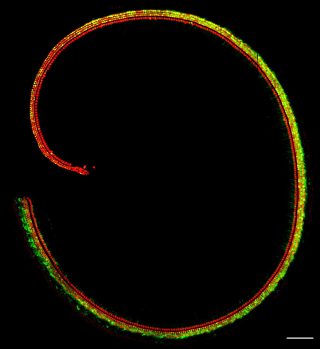
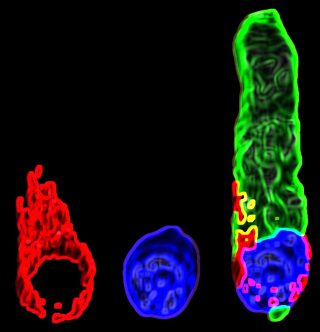
שחר טייבר: “עבדנו עם טכנולוגיה חדשנית מתחום הטיפולים הגנטיים: ייצרנו נגיף מלאכותי, שאינו גורם למחלה, והחדרנו לתוכו חומר גנטי – גרסה תקינה של הגן שפגוע במשפחות ובעכברים. הזרקנו את הנגיף לתוך האוזן הפנימית של העכברים, כך שתאי השערה נדבקו בנגיף וקלטו את החומר הגנטי שהחדרנו לו. “הדבקה” זו למעשה מתקנת את התא הפגום ומאפשרת לתאי השערה להמשיך לתפקד בצורה תקינה”.
הטיפול ניתן בסמוך ללידה, לאחר מכן החוקרים בחנו את שמיעתם של העכברים באמצעות מבחנים פיזיולוגיים והתנהגותיים. העכברים המטופלים פיתחו שמיעה תקינה, כמעט זהה לזו של עכברים רגילים ללא מוטציה. לאור הצלחת המחקר, מפתחים כעת החוקרים טיפולים דומים למוטציות נוספות שגורמות לחירשות.
פרופ׳ בני נגריס, מנהל המחלקה לרפואת אף־אוזן־גרון במרכז הרפואי מאיר וראש החוג לרפואת אף־אוזן־גרון בפקולטה לרפואה באוניברסיטת תל אביב, אשר לא היה מעורב בפרויקט, בתגובה למחקר: ״בניגוד לטיפולים המקובלים לשיפור השמיעה היום, כדוגמת מכשירי שמיעה ושתל השבלול, אשר ניתנים לאחר שהנזק כבר התהווה ומשיגים שיפור חלקי בלבד, פרופ׳ אברהם מציגה שיטה חדשנית ויעילה לטיפול בליקויי שמיעה עוד בטרם נגרם הנזק. הגישה הטיפולית שהוצגה במחקר היא פריצת דרך מחשבתית, ׳שובר שוויון׳ בטיפול בחירשות״.
המחקר נתמך בעיקר ע״י הקרן הדו-לאומית למדע ישראל-ארה״ב (BSF), המכונים הלאומיים לבריאות (NIH), מועצת המחקר האירופאית (ERC), והתכנית למחקר ברפואה ממוקדת אישית של הקרן הלאומית למדע.

